- Life
- Forschung
Meldung vom: | Verfasser/in: Maria Schulz
Wie ein Bodenbakterium zur Inspirationsquelle für neue Wirkstoffe werden kann – das zeigt eine aktuelle Studie eines interdisziplinären Forschungsteams. Durch genetische Analysen des Pflanzenpathogens Pseudomonas syringae konnten neue Einblicke in dessen chemische Vielfalt gewonnen werden. Zwei neu entdeckte Naturstoff-Familien, die Syrilipamide und Secimide, schädigen besonders in Kombination. Secimide sind zudem gegen Pilze aktiv.
Pseudomonas syringae verursacht als Erreger von Pflanzenkrankheiten große Schäden in der Landwirtschaft. Gleichzeitig produziert das Bakterium eine Vielzahl biologisch aktiver Naturstoffe. Diese könnten ihm dabei helfen, sich an wechselnde Umweltbedingungen anzupassen und Konkurrenten zu verdrängen. In einer umfassenden genomischen Analyse untersuchten die Forschenden 18 repräsentative Stämme der Bakterienart und analysierten mithilfe modernster bioinformatischer Methoden deren genetisches Potential zur Bildung von Naturstoffen.
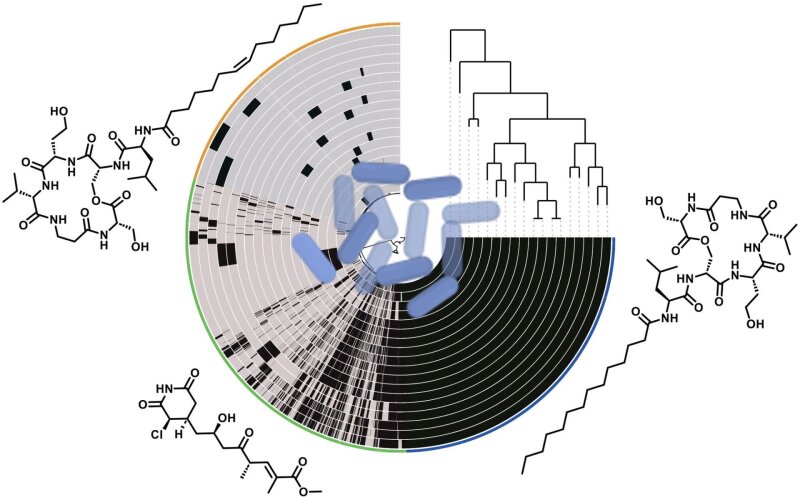
Dabei konnten sie insgesamt 231 sogenannte Biosynthese-Gencluster identifizieren. Diese Gencluster enthalten Enzym-codierende Gene, die für die Synthese von Naturstoffen zuständig sind. Besonders häufig waren Gene für Nichtribosomale Peptidsynthetasen (NRPS) vertreten. NRPS produzieren Naturstoffe, die zum Beispiel dem Bakterium helfen, sich gegen Konkurrenten durchzusetzen und sich an seine Umwelt anzupassen.
Naturstoffe mit besonderen Eigenschaften
Durch eine Kombination aus bioinformatischen Analysen, chemischer Strukturbestimmung und biologischen Aktivitätstests konnten zwei neue Naturstoff-Familien identifiziert und charakterisiert werden: Syrilipamide und Secimide. Beides sind niedermolekulare Verbindungen, die von Pseudomonas syringae gebildet werden. Diese Moleküle zeigen eine bemerkenswerte Toxizität gegenüber konkurrierenden Mikroorganismen, insbesondere Pilzen und auch Amöben. Ihre selektive Wirkung könnte zukünftig gezielt für den Schutz von Pflanzen oder als Ausgangspunkt für die Entwicklung neuer bioaktiver Substanzen genutzt werden.
Enzym SecA erweitert chemisches Repertoire
„Wir haben zudem ein bisher unbekanntes Enzym entdeckt: SecA“, sagt Shuaibing Zhang, Erstautor der Studie. „SecA fügt Chlor-Atome an bestimmte organische Verbindungen an, wodurch die strukturelle Komplexität und Aktivität der daraus entstehenden Verbindungen erhöht wird“, ergänzt Pierre Stallforth, der Leiter des Projekts. Er ist Professor an der Universität Jena und Abteilungsleiter am Leibniz-HKI. Solche chlorierten Naturstoffe spielen eine wichtige Rolle in der Pharmaforschung und könnten in Zukunft für die Entwicklung neuer Antibiotika, Krebstherapien oder Pflanzenschutzmittel genutzt werden.
Neue Perspektiven für die Biotechnologie
Mit ihrer Wirkung gegen Amöben und Pilze könnten die neu entdeckten Naturstoffe sowohl für die Landwirtschaft als auch für die pharmazeutische Forschung von Interesse sein. Zunächst einmal interessierte sich das Team jedoch für die natürliche Funktion dieser Moleküle. Sie helfen Pseudomonas syringae als vielseitigem Bakterium, Pflanzenpathogen und Produzent von bioaktiven Verbindungen bei der Verteidigung gegen Fressfeinde und Konkurrenz sowie der Nischenanpassung im natürlichen Habitat. Die Bildung von mikrobiellen Konsortien in der Natur und die Funktion der daran beteiligten Signalstoffe tragen zum Verständnis der komplexen ökologischen Wechselwirkungen in unserer Umwelt bei und sind Forschungsschwerpunkt des Jenaer Exzellenzclusters „Balance of the Microverse“Externer Link. An der Arbeit waren Wissenschaftler*innen des Leibniz-Instituts für Naturstoff-Forschung und Infektionsbiologie – Hans-Knöll-Institut (Leibniz-HKI) und der Friedrich-Schiller-Universität Jena beteiligt.
Das Projekt wurde durch die Werner Siemens-Stiftung, die Leibniz-Gemeinschaft und die Deutsche Forschungsgemeinschaft im Rahmen des Sonderforschungsbereichs ChemBioSys und des Exzellenzclusters „Balance of the Microverse“ gefördert.
Die Pangenomanalyse von Pseudomonas-syringae-Stämmen (Mitte) hat es ermöglicht, neue Verbindungen zu finden (außen).
Grafik: Luo Yu, Leibniz-HKIOriginal-Publikation:
Zhang S, Huang Y, Nachawati R, Huber P, Walther G, Gregor L, Vilotijević I, Stallforth P (2025) Pangenome Analysis of the Plant Pathogen Pseudomonas syringae Reveals Unique Natural Products for Niche Adaptation. Angew Chem Int Ed 64 (25), e202503679, https://doi.org/10.1002/anie.202503679Externer Link
Kontakt:
07745 Jena Google Maps – LageplanExterner Link